Contente
- Câncer de mama hereditário
- Mutações do gene não BRCA
- Câncer de mama e testes genéticos
- Suporte para câncer de mama hereditário
Além das mutações nos genes BRCA1 e BRCA2, algumas delas incluem mutações em ATM, PALB2, PTEN, CDH1, CHEK2, TP53, STK11, PMS2 e mais. Vejamos como essas mutações não BRCA1 / BRCA2 são importantes no câncer de mama familiar e algumas das características daquelas mais comumente encontradas.
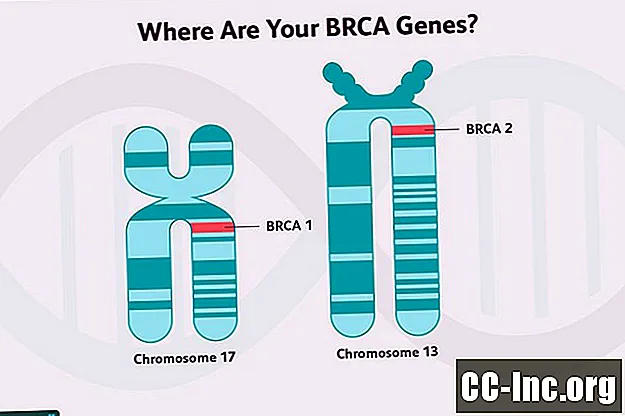
Câncer de mama hereditário
Atualmente, acredita-se que 5% a 10% dos cânceres de mama sejam genéticos ou familiares (embora esse número possa mudar à medida que aprendemos mais), mas nem todos esses cânceres são causados por mutações BRCA.
No máximo, 29% (e provavelmente muito menos) dos cânceres de mama hereditários testam positivo para as mutações do gene BRCA1 ou BRCA2, e muitas pessoas estão realizando testes para outras alterações genéticas conhecidas.
Uma vez que a ciência por trás do câncer hereditário é muito provocadora de ansiedade, para não falar em confusa e incompleta, é útil começar falando sobre a biologia das mutações genéticas e como essas mudanças no DNA desempenham um papel no desenvolvimento do câncer.
Mutações genéticas herdadas vs. adquiridas
Ao falar sobre mutações, é importante distinguir entre mutações genéticas herdadas e adquiridas.
Mutações genéticas adquiridas ou somáticas têm recebido muita atenção nos últimos anos, pois essas mutações causam mudanças que impulsionam o crescimento do câncer. As terapias direcionadas, drogas que visam vias específicas relacionadas a essas mudanças, melhoraram significativamente o tratamento de alguns tipos de câncer, como o de pulmão.
Mutações adquiridas, no entanto, não estão presentes desde o nascimento, mas sim, são formadas a qualquer momento após o nascimento, no processo de uma célula se tornar uma célula cancerosa. Essas mutações afetam apenas algumas células do corpo. Eles não são herdados de um dos pais, mas sim "adquiridos" à medida que o DNA das células é exposto a danos ambientais ou como resultado dos processos metabólicos normais do corpo.
Em contraste, mutações herdadas ou da linha germinativa são alterações genéticas com as quais as pessoas nascem e que são transmitidas por um ou ambos os pais. Essas mutações afetam todas as células do corpo. São essas mutações herdadas (e outras alterações genéticas) que podem aumentar a chance de uma pessoa desenvolver câncer e são responsáveis pelo que é conhecido como câncer de mama hereditário ou familiar.
Mutações genéticas hereditárias (linha germinativa) vs. adquiridas (somáticas)Como as mutações genéticas hereditárias aumentam o risco de câncer?
Muitas pessoas se perguntam como exatamente um gene anormal ou combinações de genes podem levar ao câncer de mama, e uma breve discussão da biologia é útil para entender muitas das questões, como por que nem todos que têm essas mutações desenvolvem câncer.
Nosso DNA é um projeto ou código usado para fabricar proteínas. Quando o mapa ou código está errado (como as "letras" em um determinado gene), ele fornece instruções erradas para a síntese de uma proteína. A proteína anormal é então incapaz de realizar seu trabalho normal. Nem todas as mutações genéticas aumentam o risco de câncer e, de fato, a maioria não aumenta. Mutações nos genes responsáveis pelo crescimento e divisão das células, ou "mutações condutoras", são o que impulsiona o crescimento dos cânceres. Existem dois tipos principais de genes que, quando sofrem mutação, podem levar ao crescimento descontrolado conhecido como câncer: oncogenes e genes supressores de tumor.
Vários dos genes associados a um maior risco de câncer de mama são genes supressores de tumor. Esses genes codificam proteínas que funcionam para reparar danos ao DNA nas células (danos de toxinas no ambiente ou processos metabólicos normais nas células), servem para eliminar células que não podem ser reparadas ou regular o crescimento de outras maneiras. Os genes BRCA1 e BRCA2 são genes supressores de tumor.
Muitos desses genes são autossômicos recessivos, o que significa que cada pessoa herda uma cópia do gene de cada pai, e ambas as cópias devem sofrer mutação para aumentar o risco de câncer. De forma simplista, isso significa que uma combinação de fatores genéticos e ambientais (uma mutação adquirida no outro gene) precisa agir em conjunto para resultar no desenvolvimento do câncer. Somado a isso, normalmente, várias mutações devem ocorrer para que uma célula se torne uma célula cancerosa.
O que significa ter uma predisposição genética para o câncerGene Penetrance
Nem todas as mutações genéticas ou alterações genéticas aumentam o risco de câncer de mama no mesmo grau, e este é um conceito importante para qualquer pessoa que esteja considerando o teste genético, especialmente porque muitas pessoas já ouviram falar do risco muito alto conferido pelas mutações BRCA. A penetrância do gene é definida como a proporção de pessoas com uma mutação que irão apresentar a doença (neste caso, desenvolver câncer de mama).
Para algumas mutações, o risco de câncer de mama é muito alto. Para outros, o risco pode ser aumentado por apenas um fator de 1,5. É importante entender isso ao falar sobre as possíveis opções preventivas.
Epigenética
Outro conceito importante para a compreensão da genética e do câncer, embora muito complexo para explorar em detalhes aqui, é o da epigenética. Aprendemos que as mudanças no DNA que não envolvem mudanças nos pares de bases (nucleotídeos) ou nas "letras" que codificam uma proteína podem ser tão importantes no desenvolvimento do câncer. Em outras palavras, em vez de mudanças estruturais na espinha dorsal do DNA, pode haver mudanças moleculares que mudam a forma como a mensagem é lida ou expressa.
Mutações do gene não BRCA
As mutações do gene BRCA são as anomalias genéticas mais conhecidas associadas ao câncer de mama, mas está claro que existem mulheres com predisposição ao câncer de mama com base em seu histórico familiar, cujo teste é negativo.
Um estudo de 2017 descobriu que as mutações do BRCA eram responsáveis por apenas 9% a 29% dos cânceres de mama hereditários. Mesmo quando o teste foi feito para outras 20 a 40 mutações conhecidas, no entanto, apenas 4 a 11% das mulheres testaram positivo. Em outras palavras, 64% a 86% das mulheres com suspeita de câncer de mama hereditário tiveram resultados negativos para ambas as mutações BRCA e 20 a 40 outras.
Câncer de mama familiar não BRCA1 / BRCA2
Nosso conhecimento sobre as mutações genéticas que aumentam o risco de câncer de mama ainda é incompleto, mas agora sabemos que existem pelo menos 72 mutações genéticas ligadas ao câncer de mama hereditário. Acredita-se que essas mutações (e outras ainda não descobertas) sejam responsáveis por 70 a 90 por cento dos cânceres de mama hereditários com resultado negativo para mutações do gene BRCA. O acrônimo BRCAX foi cunhado para descrever essas outras mutações, que significa não BRCA1 Câncer de mama familiar relacionado ao BRCA2.
72 mutações genéticas ligadas ao câncer de mama hereditárioAs anormalidades genéticas abaixo diferem em sua frequência, na quantidade de risco associado, no tipo de câncer de mama ao qual estão associadas e em outros cânceres associados às mutações.
A maioria desses cânceres de mama tem características semelhantes (como tipo de câncer, status do receptor de estrogênio e status HER2) aos cânceres de mama não hereditários ou esporádicos, mas há exceções. Por exemplo, algumas mutações estão mais fortemente associadas ao câncer de mama triplo negativo, incluindo mutações em BARD1, BRCA1, BRCA2, PALB2, eRAD51D.
Variabilidade dentro de mutações
Nem todas as pessoas que apresentam as seguintes mutações genéticas são iguais. Em geral, pode haver centenas de maneiras pelas quais esses genes sofrem mutação. Em alguns casos, o gene produzirá proteínas que suprimem o crescimento do tumor, mas as proteínas não funcionarão tão bem quanto a proteína normal. Com outras mutações, a proteína pode não ser produzida.
BRCA (uma breve revisão para comparação)
As mutações do gene BRCA 1 e do gene BRCA2 estão ambas associadas a um risco aumentado de desenvolver câncer de mama, assim como alguns outros tipos de câncer, embora as duas difiram um pouco nesse risco.
Em média, 72% das mulheres que têm mutações BRCA1 e 69% que têm genes BRCA2 mutados desenvolverão câncer de mama aos 80 anos.
Além disso, os cânceres de mama associados a essas mutações podem ser diferentes. O câncer de mama em mulheres com mutações no BRCA1 tem maior probabilidade de ser triplo negativo. Cerca de 75% são receptores de estrogênio negativos e também têm menos probabilidade de serem HER2 positivas. Eles também são mais propensos a ter um grau de tumor mais alto. Os cânceres de mama em mulheres com mutações BRCA2, em contraste, são semelhantes aos cânceres em mulheres que não são portadoras da mutação do gene BRCA.
Gene ATM (ATM Serine / Threonine Kinase)
O gene ATM codifica proteínas que ajudam a controlar a taxa de crescimento das células. Eles também auxiliam no reparo de células danificadas (células que sofreram danos no DNA de toxinas), ativando enzimas que reparam esses danos.
Aqueles que têm duas cópias do gene mutado têm uma síndrome autossômica recessiva incomum conhecida como ataxia-telangiectasia. Com a ataxia-telangiectasia, as proteínas defeituosas não só aumentam o risco de câncer, mas também resultam na morte precoce de algumas células do cérebro, resultando em um distúrbio neurodegenerativo progressivo.
Pessoas que têm apenas uma cópia mutada do gene (cerca de 1% da população) têm um risco vitalício de desenvolver câncer de mama de 20% a 60%.
Acredita-se que as pessoas com essa mutação sejam predispostas ao câncer de mama em uma idade precoce, bem como a desenvolver câncer de mama bilateral.
O rastreamento do câncer de mama com ressonâncias magnéticas de mama é recomendado a partir dos 40 anos, e as mulheres podem considerar mastectomias preventivas. Pessoas com um gene ATM mutado também parecem ter predisposição a cânceres de tireoide e pancreático e são mais sensíveis à radiação.
PALB2
Mutações no gene PALB2 também são uma causa importante de câncer de mama hereditário. O gene PALB2 codifica uma proteína que funciona em conjunto com a proteína BRCA2 para reparar o DNA danificado nas células. No geral, o risco ao longo da vida de câncer de mama com uma mutação PALB2 é tão alto quanto 58 por cento, embora possa variar com a idade. O risco é de 8 a 9 vezes a média para mulheres com menos de 40 anos, mas cerca de 5 vezes a média para mulheres com mais de 60 anos.
Entre aquelas que carregam uma cópia do gene, 14% desenvolverão câncer de mama aos 50 anos e 35% aos 70 (menos do que com as mutações BRCA).
Pessoas que têm a mutação PALB2 e desenvolvem câncer de mama podem ter um risco maior de morrer da doença.
Pessoas que herdam 2 cópias do gene PALB2 mutado têm um tipo de anemia Fanconi caracterizada por contagens muito baixas de glóbulos vermelhos, glóbulos brancos e plaquetas.
CHEK2
O gene CHEK2 codifica uma proteína que é ativada quando ocorre dano ao DNA. Ele também ativa outros genes envolvidos no reparo celular.
Os riscos ao longo da vida para portadores de mutações truncadas CHEK2 são de 20 por cento para uma mulher sem nenhum parente afetado, 28 por cento para uma mulher com um parente de segundo grau afetado, 34 por cento para uma mulher com um parente de primeiro grau afetado e 44 por cento para uma mulher com um parente de primeiro e segundo grau afetado.
Para homens e mulheres, o gene também aumenta o risco de câncer de cólon e linfoma não-Hodgkin.
CDH1
As mutações no CDH1 causam uma condição conhecida como síndrome do câncer gástrico hereditário.
Pessoas que herdam este gene têm um risco vitalício de até 80% de desenvolver câncer de estômago e de até 52% de desenvolver câncer de mama lobular.
O gene codifica uma proteína (caderina epitelial) que ajuda as células a se prenderem (uma das diferenças entre as células cancerosas e as normais é que as células cancerosas não possuem esses produtos químicos de adesão que as fazem grudar). Os cânceres em pessoas que herdam essa mutação têm maior probabilidade de metástase.
PTEN
As mutações no gene PTEN são uma das mutações do gene supressor de tumor mais comuns. O gene codifica proteínas que regulam o crescimento das células e também ajuda as células a se unirem.
Mutações no gene parecem aumentar o risco de células cancerosas se separarem de um tumor e metastatizarem. O PTEN está associado a uma síndrome chamada síndrome do tumor hamartoma PTEN, bem como à síndrome de Cowden.
As mulheres que carregam uma mutação PTEN têm um risco vitalício de desenvolver câncer de mama de até 85 por cento e também têm um risco aumentado de alterações benignas da mama, como doença fibrocística, adenose e papilomatose intraductal.
As mutações também estão associadas a um risco aumentado de câncer uterino (e miomas uterinos benignos), câncer de tireoide, câncer de cólon, melanoma e câncer de próstata.
Os sintomas não relacionados ao câncer incluem cabeça grande (macrocefalia) e a tendência de formar tumores benignos conhecidos como hamartomas.
STK11
Mutações no STK11 estão associadas a uma condição genética conhecida como síndrome de Peutz-Jegher. STK11 é um gene supressor de tumor envolvido no crescimento celular.
Além de um risco aumentado de câncer de mama (com risco ao longo da vida de até 50 por cento), a síndrome carrega um risco aumentado de muitos tipos de câncer, alguns dos quais incluem câncer de cólon, câncer de pâncreas, câncer de estômago, câncer de ovário, câncer de pulmão, câncer uterino e muito mais.
Condições não relacionadas ao câncer associadas à mutação incluem pólipos não cancerígenos no trato digestivo e no sistema urinário, sardas no rosto e no interior da boca e muito mais. O rastreamento do câncer de mama é frequentemente recomendado para mulheres a partir dos 20 anos, e frequentemente com ressonância magnética com ou sem mamografias.
TP53
O gene TP53 codifica proteínas que impedem o crescimento de células anormais.
Essas mutações são extremamente comuns no câncer, com adquirido mutações no gene p53 sendo encontradas em cerca de 50 por cento dos cânceres.
Mutações hereditárias são menos comuns e estão associadas a doenças conhecidas como síndrome de Li-Fraumeni ou síndrome semelhante a Li-Fraumeni (que apresenta menor risco de câncer). A maioria das pessoas que herdam a mutação desenvolve câncer aos 60 anos e, além do câncer de mama, está propensa a desenvolver câncer ósseo, adrenal, pancreático, de cólon, de fígado, de cérebro, de leucemia e muito mais. Não é incomum que pessoas com a mutação desenvolvam mais de um câncer primário.
Acredita-se que mutações herdadas no gene p53 sejam responsáveis por cerca de 1% dos casos de câncer de mama hereditário. Os cânceres de mama associados à mutação costumam ser HER2 positivos e apresentam alto grau de tumor.
Síndrome de Lynch
A síndrome de Lynch ou câncer colorretal hereditário sem polipose está associado a mutações em vários genes diferentes, incluindo PMS2, MLH1, MSH2, MSH6 e EPCAM.
O PMS2, em particular, foi associado ao dobro do risco de câncer de mama. O gene funciona como um gene supressor de tumor, codificando uma proteína que repara o DNA danificado.
Além do câncer de mama, essas mutações apresentam um alto risco de câncer de cólon, ovário, útero, estômago, fígado, vesícula biliar, intestino delgado, rim e cérebro.
Outras Mutações
Existem várias outras mutações genéticas associadas a um risco aumentado de desenvolver câncer de mama e espera-se que mais sejam descobertas em um futuro próximo. Alguns deles incluem:
- BRIP1
- BARD1
- MRE11A
- NBN
- RAD50
- RAD51C
- SEC23B
- BLM
- MUTYH
Câncer de mama e testes genéticos
No momento, o teste está disponível para mutações do gene BRCA, bem como mutações ATM, CDH1, CHEK2, MRE11A, MSH6, NBN, PALB2, PMS2, PTEN, RAD50, RAD51C, SEC23B e TP53, com esta área prevista para expandir dramaticamente no futuro próximo.
Ter esses testes disponíveis, entretanto, levanta muitas questões. Por exemplo, quem pode ter câncer de mama hereditário e quem deve ser testado? O que você deve fazer se o teste for positivo para um desses genes?
Idealmente, qualquer teste deve ser feito apenas com a orientação e ajuda de um conselheiro genético. Há duas razões para isso.
Uma delas é que pode ser devastador saber que você carrega uma mutação que pode aumentar seu risco, e a orientação de alguém que conhece o tratamento recomendado e a triagem é inestimável.
Conforme observado anteriormente, algumas mutações conferem um alto risco e outras um risco muito menor. Algumas mutações podem ser mais preocupantes no início da vida (digamos, na casa dos 20 anos), enquanto outras podem não exigir exames precoces. Um conselheiro genético pode ajudá-lo a aprender sobre o que é atualmente recomendado com relação ao rastreamento de sua mutação específica, levando em consideração quaisquer outros fatores de risco que você possa ter.
A outra razão pela qual o aconselhamento genético é tão importante é que você pode ter um risco significativo de desenvolver câncer de mama, mesmo que seus testes sejam negativos. Ainda há muito a aprender, e um conselheiro genético pode ajudá-lo a examinar a história de sua família para ver se você corre um risco alto apesar do teste negativo, e planejar o rastreamento de acordo.
Teste genético para câncer de mamaSuporte para câncer de mama hereditário
Assim como as pessoas que foram diagnosticadas com câncer de mama precisam de apoio, aquelas que carregam genes que aumentam o risco precisam de apoio. Felizmente, existem organizações que se concentram especificamente em apoiar pessoas nessa situação.
Uma organização, FORCE, que é um acrônimo para Facing Our Risk of Cancer Empowered, oferece uma linha de ajuda, quadro de mensagens e informações para aqueles que estão enfrentando câncer hereditário.
Outras organizações e comunidades de apoio estão disponíveis para ajudar as pessoas a lidar com as decisões relacionadas ao diagnóstico de câncer de mama hereditário.
O termo "previvor" foi cunhado pela FORCE para descrever pessoas que estão sobrevivendo à predisposição ao câncer de mama. Se esta é a situação que você está enfrentando, você não está sozinho e, usando a hashtag #previvor, poderá encontrar muitas outras no Twitter e em outras mídias sociais.
Uma palavra de Verywell
Pode ser opressor aprender sobre as muitas mutações genéticas diferentes que aumentam o risco de câncer de mama além das mutações BRCA, mas essas "outras" mutações são de importância significativa, sabendo que as mutações BRCA são responsáveis por uma minoria relativa dos cânceres de mama familiares. Ao mesmo tempo, a ciência que analisa o câncer de mama hereditário ainda está em sua infância e há muito a aprender. Se você está preocupado com a possibilidade de ter uma mutação ou descobriu que sim, é útil aprender o máximo que puder. Organizações de câncer hereditário como a FORCE podem não apenas fornecer mais informações, mas também ajudá-lo a se conectar com outras pessoas que estão enfrentando uma jornada com questões e preocupações semelhantes.